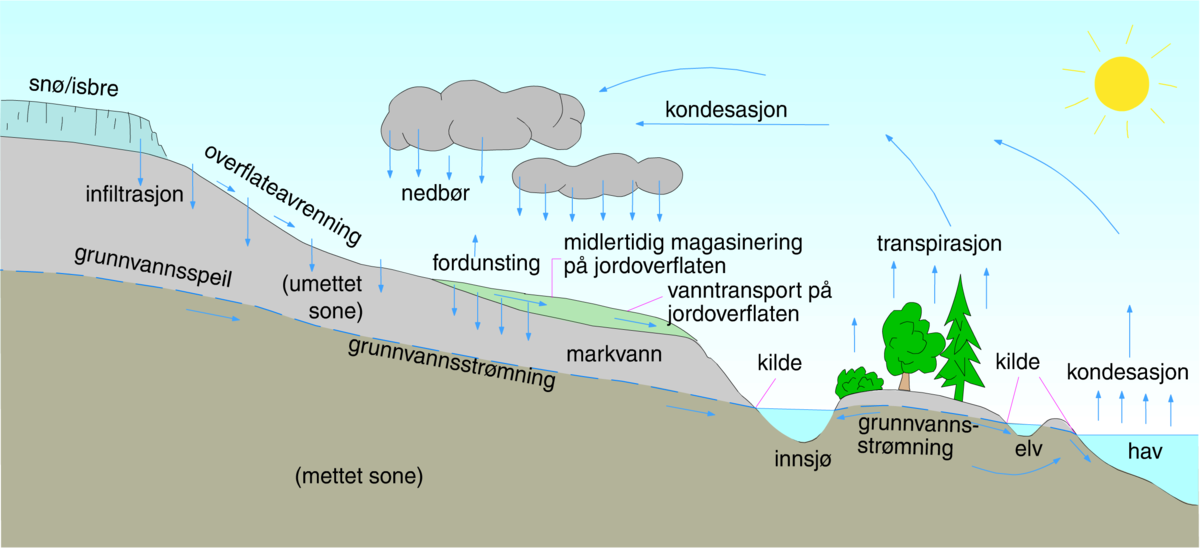
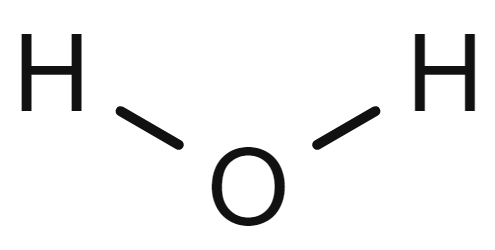
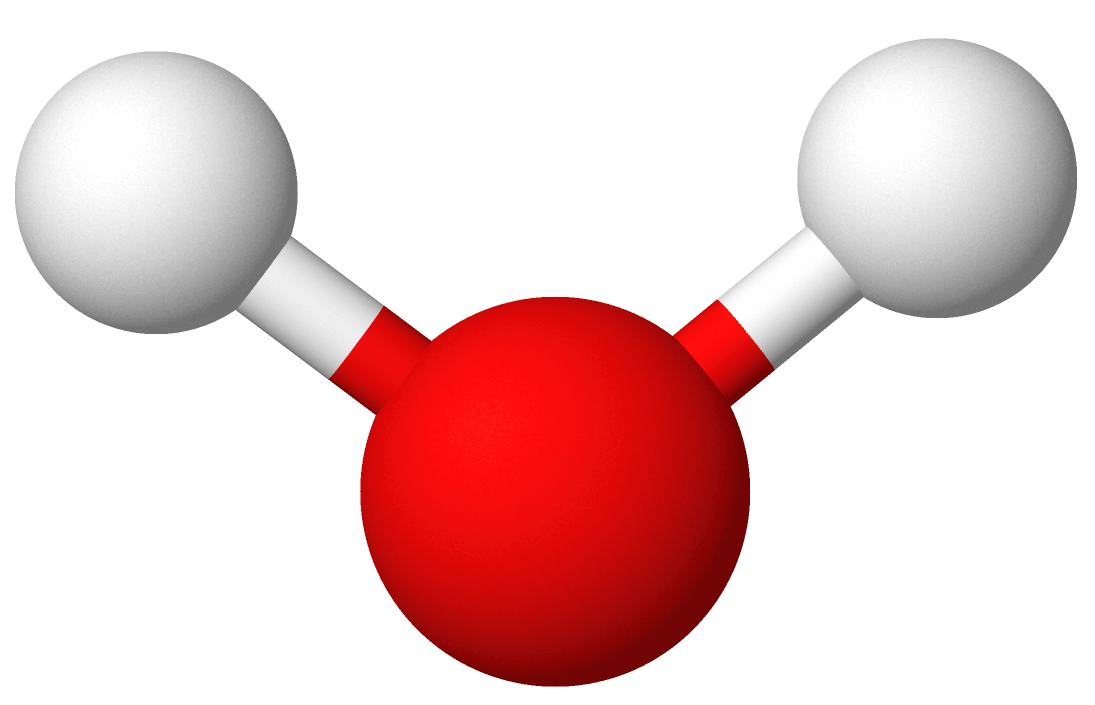
Vatn er ein kjemisk forbindelse mellom hydrogen og oksygen med strukturformel H2O. Vatn er den mest utbreidde og brukte kjemiske sambindinga på overflata av planeten jorda.
Faktaboks
- Norsk namn
- vatn, vann
- Engelsk namn
- water
- Også kjend som
-
vass- (i sammensette ord), latin: aqua
- Kjemisk formel
-
H2O
- Stoffklasse
- uorganisk molekyl
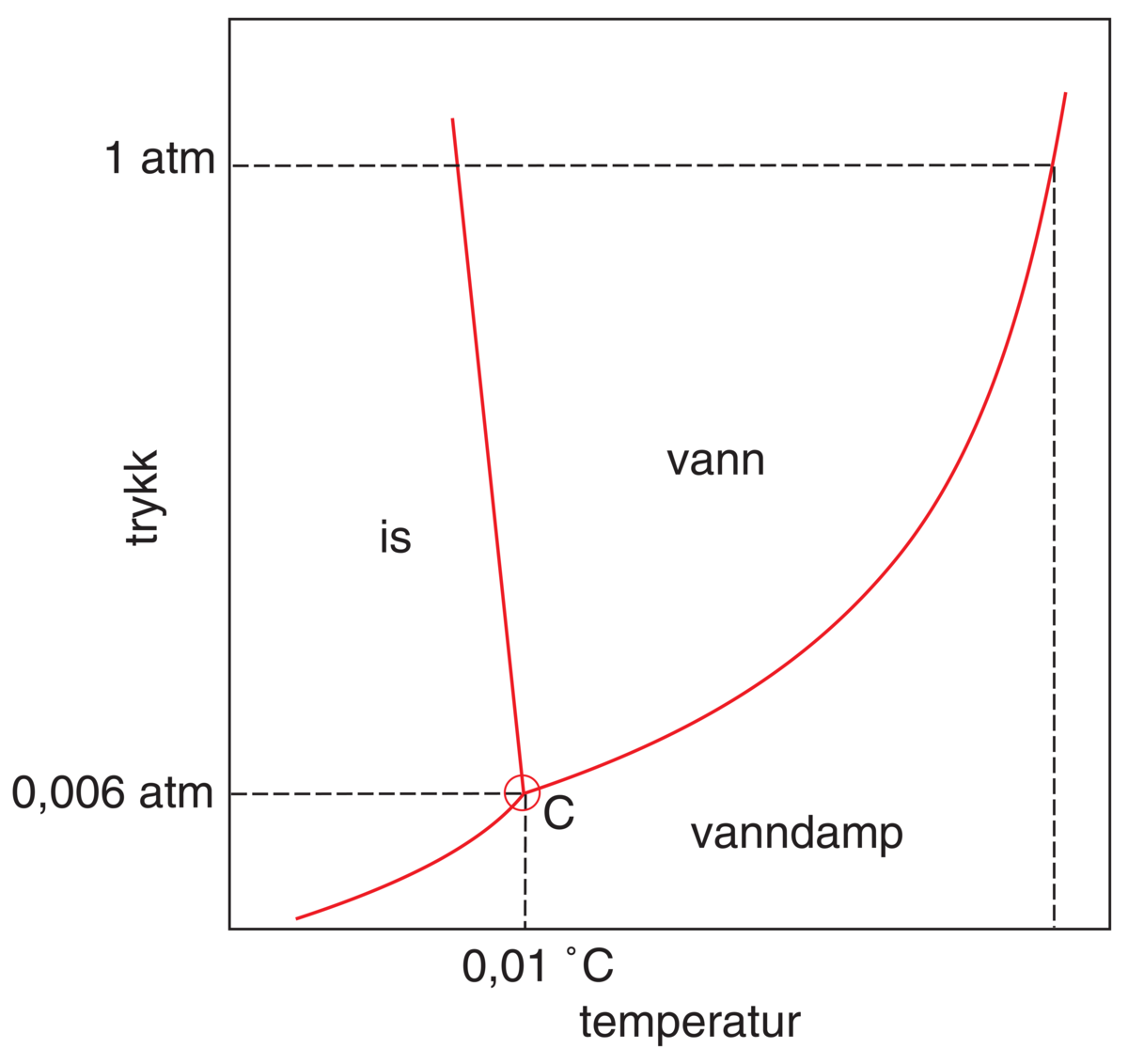
- Smeltepunkt
- 0 °C
- Kokepunkt
- 100 °C
- Tilstand
- væske
Vanlegvis blir orda vatn brukt om forbindelsen i flytande form, men her vil vi òg bruke orda vatn om is, snø og vassdamp. Vatn finst som væske (flytande vatn), i fast form (is) eller som gass (vassdamp). Vassmolekyla er stadig i rørsle, og vatnet skiftar form etter kor rask rørsle molekyla har. Når vatn blir varma opp, blir det tilført energi, noko som set vassmolekyla i rørsle, og hydrogenbindingane blir brotne. Vatnet går då frå væskeform til gassform. Vassdamp er vassmolekyl som smett ut av vatnet og ut i lufta. Når vassdampen blir avkjølt, endrar han seg og blir til flytande væske igjen. Dette heiter at dampen kondenserer.
Mange av dei kjemiske reaksjonane som går føre seg på jorda og i oss menneske og alt anna levande, involverer vatn eller går føre seg løyst i vatn. Sjå vatn – fysiologi.
Vatn har òg hatt stor betydning for historien og har ulik tyding i ulike kulturar og religionar. Sjå vatn – religion.









Kommentarar
Kommentarar til artikkelen blir synleg for alle. Ikkje skriv inn sensitive opplysningar, for eksempel helseopplysningar. Fagansvarleg eller redaktør svarar når dei kan. Det kan ta tid før du får svar.
Du må være logga inn for å kommentere.