Et polart molekyl er et molekyl med et permanent elektrisk dipolmoment.
Faktaboks
- Uttale
- polˈart molekˈyl
I et molekyl som A–B, vil tyngdepunktet for negativ og positiv ladning ikke falle sammen på grunn av forskjellen i elektronegativitet mellom A og B, og molekylet vil være et polart molekyl.
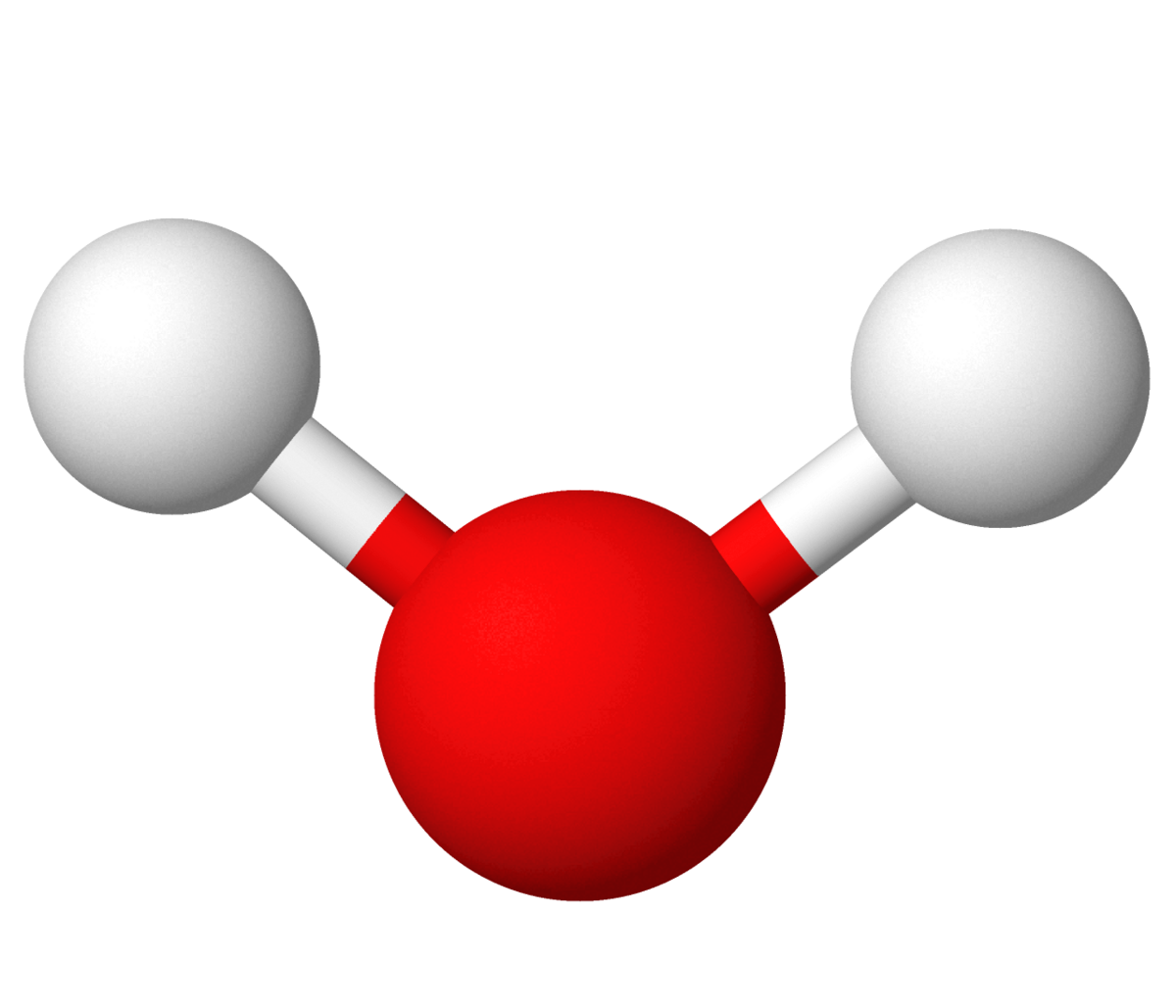
Hver av de to O–H-bindingene i et vannmolekylet, H–O–H, er polare. Da molekylet er vinklet er det som helhet polart.
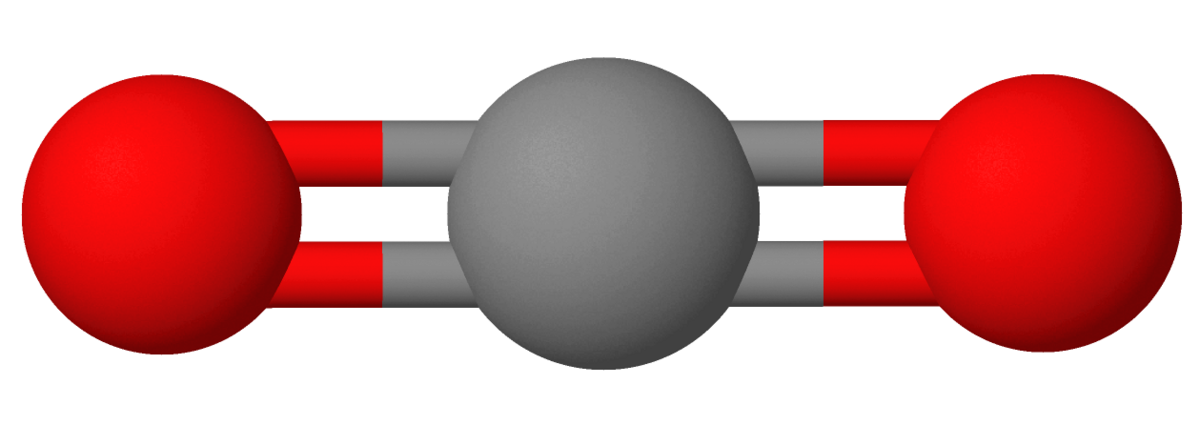
I karbondioksidmolekylet, O=C=O, er hver av de to C=O-bindingene polare, men da molekylet er lineært og sentrosymmetrisk, vil de to dipolene oppheve hverandre, og CO2 har ikke noe dipolmoment.




Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.