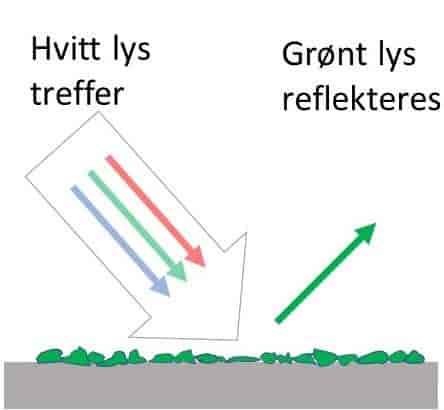
Klorofyll er et grønt pigment som er nødvendig for fotosyntese. Klorofyll-molekylene trengs til å fange energi fra sollys og omdanne den til kjemisk energi, som senere brukes til karbonfiksering. Klorofyll finnes i tylakaidmembranene i kloroplastene i planteceller, og i noen typer bakterier.
Klorofyll dannes bare i lys og når de nødvendige mineralstoffene (som nitrogen, magnesium, jern, mangan og andre) er til stede. Dersom et av disse stoffene mangler, oppstår klorose. Kimplanter av nakenfrøete planter kan danne klorofyll også i mørke.
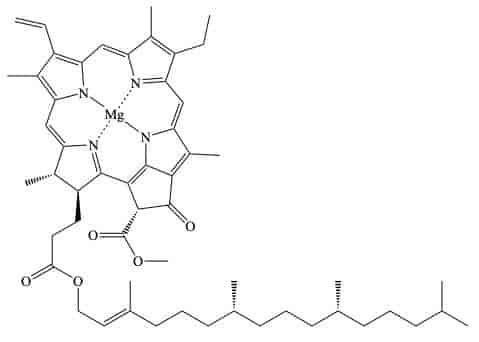
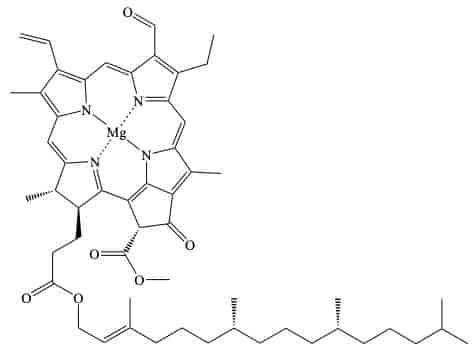
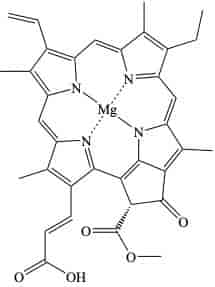
Det finnes flere typer klorofyll i plantene og de andre organismene som har fotosyntese. Ulike typer klorofyll absorberer forskjellige bølgelengder lys. Dette gir karakteristiske absorpsjonsspektra, som viser hvilke deler av lysspekteret som absorberes mest.
Klorofyll brukes som grønt fargestoff i næringsmidler, E 140.






Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.