Aminosyrer er organiske molekyler som har to stabile grupper av atomer til felles, aminogruppen og syregruppen.
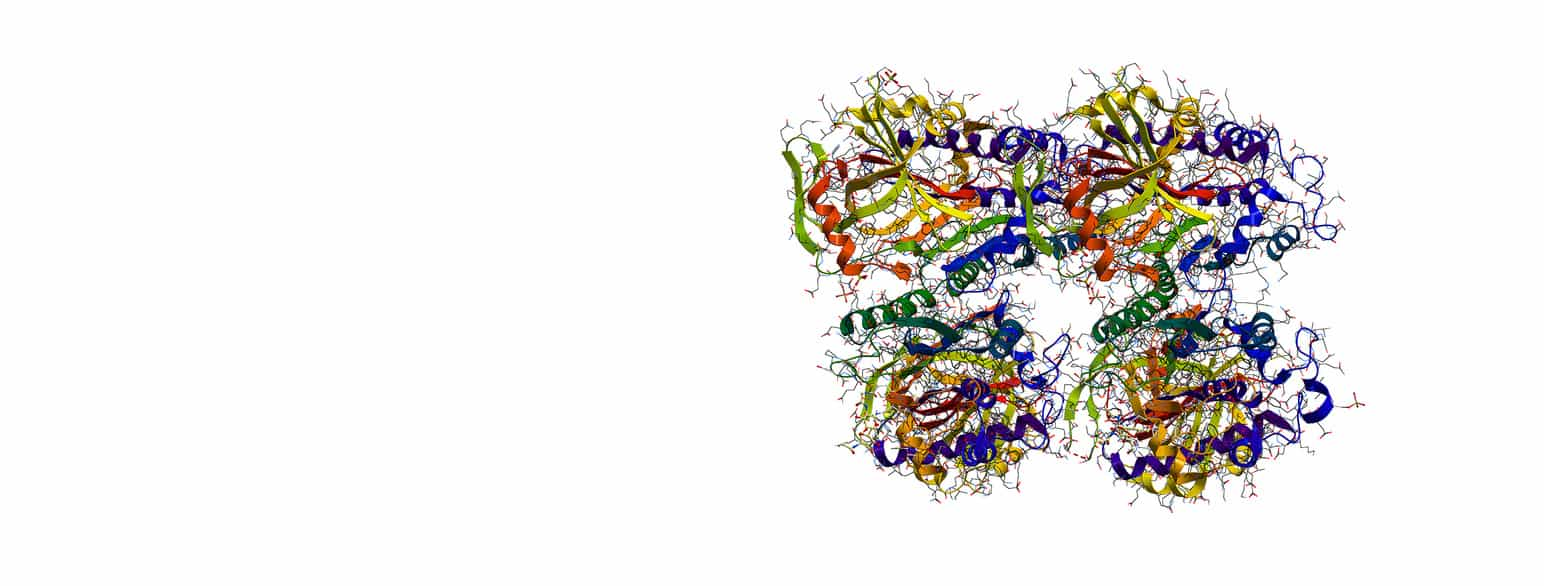
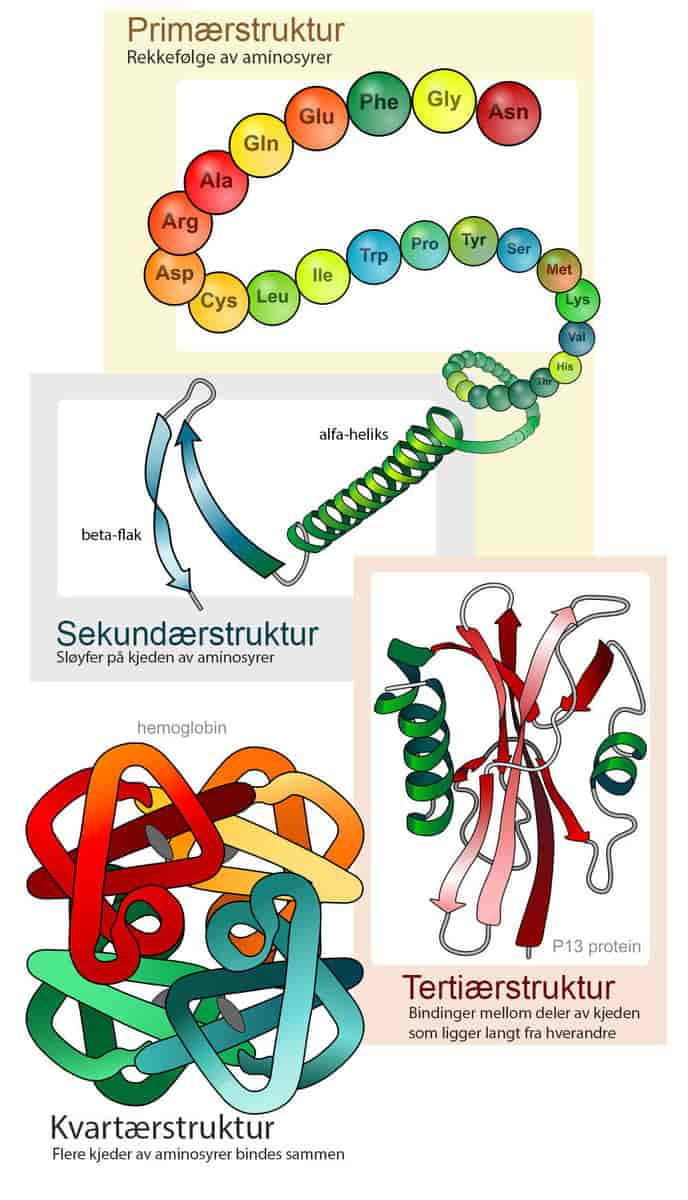
De viktigste aminosyrene er de 20 som brukes som byggemateriale for proteiner i levende organismer. En aminosyre kan da sammenlignes med en byggekloss som det finnes 20 forskjellige utgaver av. Disse aminosyrene kan kjedes sammen. Genene inneholder oppskrifter på hvilken rekkefølge aminosyrene skal kjedes sammen i gjennom proteinsyntesen. Når disse kjedene foldes i rett struktur, utgjør de proteiner.
Bare planter er i stand til å lage alle de 20 aminosyrene. Dyr, inkludert mennesker, kan lage omtrent halvparten av dem, og resten må de skaffe seg fra planter. De aminosyrene mennesket må skaffe seg gjennom kosten kalles essensielle aminosyrer. Det er ni essensielle aminosyrer. De elleve aminosyrene som mennesket kan lage selv kalles ikke-essensielle.
Alle aminosyrer inneholder atomer av karbon, hydrogen, oksygen og nitrogen; noen viktige aminosyrer inneholder dessuten svovel.
Strukturformelen til en aminosyre er: RCH(NH2)COOH, der COOH er syregruppen og NH2 er aminogruppen. Disse to gruppene er felles for aminosyrene. R står for restgruppe, og denne er ulik for hver av aminosyrene.


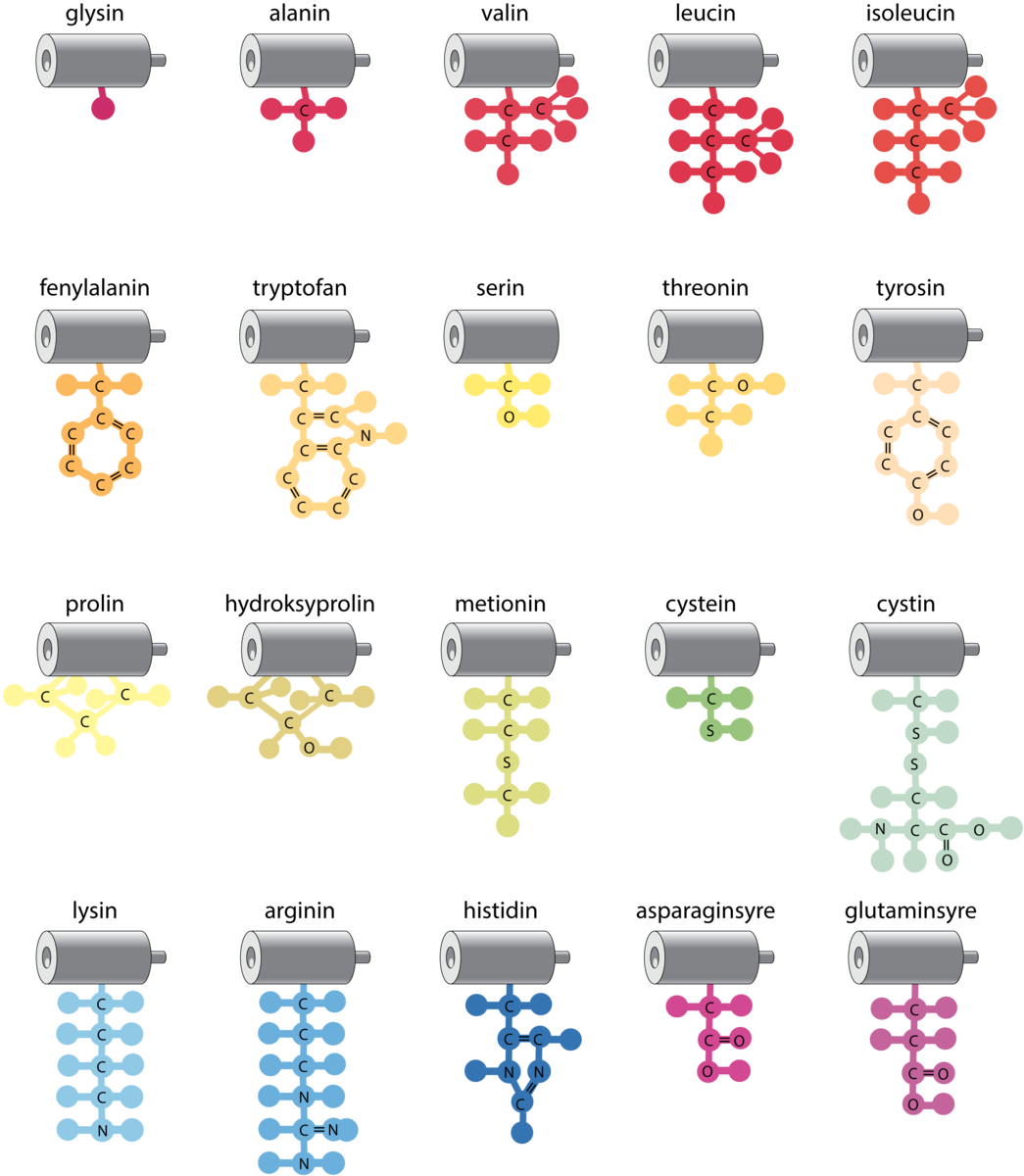
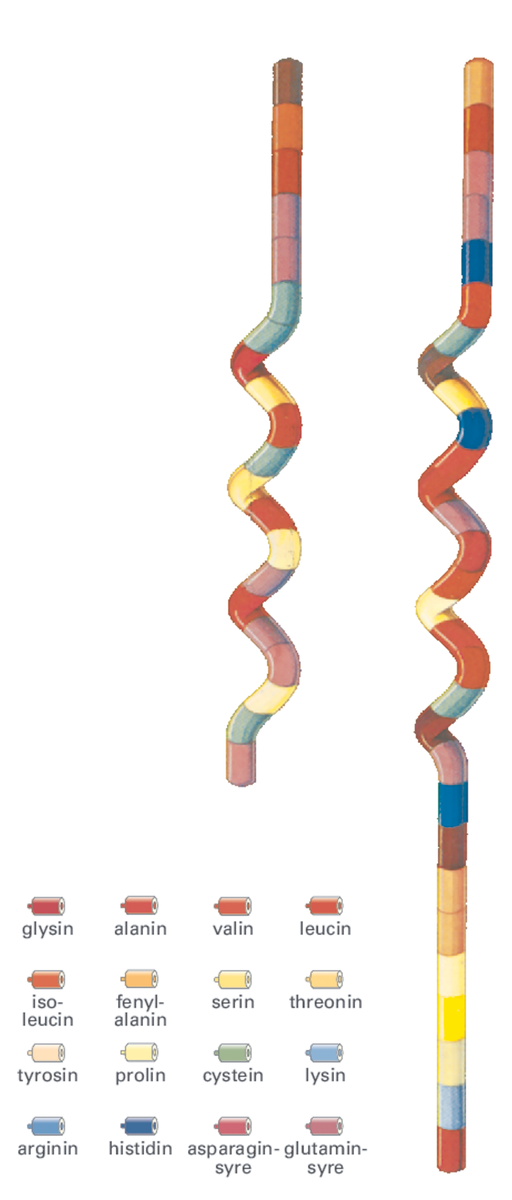



Kommentarer (7)
skrev Maj-Brit Engene
skrev Halvard Bysheim
svarte Thale Kristin Olsen
skrev Jonas Ekerhovd
Er ikke histidin klassifisert som en av de essentielle aminosyrene? Alle andre kilder jeg har lest mener at den er blant de 9 (ikke 8) vi må få via mat både for voksne og spedbarn.
svarte Halvard Hiis
Hei. Jo, du har rett. Artikkelen er nå oppdatert av en fagansvarlig. Takk for kommentaren. Vennlig hilsen Halvard Hiis
svarte Christine Wasa
Det står fortsatt 8 essensielle noen steder i teksten og 9 andre. Står altså to ulike ting i teksten etter rettingen
svarte Halvard Hiis
Takk for at du minner om dette, Christine. Jeg ser at det er flere steder i leksikonet hvor dette ikke er oppdatert. Jeg skal gå gjennom og lete opp så det blir konsistent. Det er bra med slike innspill! Vennlig hilsen Halvard
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.