Histidin er en av de 20 aminosyrene som brukes for å lage proteiner. Den er en essensiell aminosyre, som betyr at mennesker ikke er i stand til å lage aminosyren i kroppen, men må få den tilført via kosten.
Faktaboks
- Uttale
- histidˈin
Histidin er en av de 20 aminosyrene som brukes for å lage proteiner. Den er en essensiell aminosyre, som betyr at mennesker ikke er i stand til å lage aminosyren i kroppen, men må få den tilført via kosten.
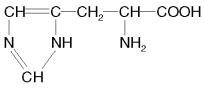
Histidin har en aromatisk sidekjede som kalles imidazol. Imidazol er bygget som en femkant med tre karbonatomer og to nitrogenatomer.
Den aromatiske sidekjeden er i stand til å lage mange typer forbindelser med andre atomer og molekyler. Det gjør at histidin ofte blir brukt i det aktive setet i enzymer. Spesielt viktig er histidins evne til å lage forbindelser med metallioner, som ofte er kofaktorer for enzymene.
Et eksempel på histidins evne til å virke med metallioner er i sink-fingre. Sink-fingre er en gruppe med lignende rekkefølger av aminosyrer i proteiner som trenger ett eller flere sink-ioner for å fungere. Det finnes mange forskjellige typer sink-fingre, men hos flesteparten av dem er det histidin som binder til seg sink-ionet.
Et annet eksempel er det oksygenbærende fargestoffet hemoglobin i de røde blodcellene som bruker jern-ioner til å ta opp og holde på oksygen. Jern-ionet binder seg til histidin. Når jernet får oksygen festet til seg, så flytter den seg og histidinet følger etter. Dette endrer strukturen til hemoglobinet slik at de andre plassene lettere kan ta opp oksygen. På den måten kan hemoglobinet ta opp mye oksygen når den kommer til et miljø med oksygen til stede.
Histidin tjener også som et forstadium til histamin, som er et viktig i signalstoff blant annet immunforsvaret. For å gjøre om histidin til histamin så blir det fjernet ett karbonatom og to oksygenmolekyler i form av karbondioksid ved hjelp av et enzym.
Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.