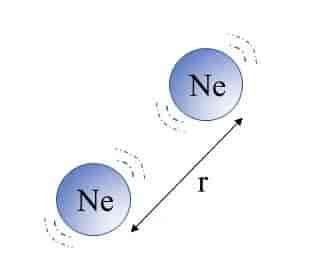
Noen atomer har fulle elektronskall, er elektriske nøytrale og har liten evne til å vekselvirke med andre atomer. Imidlertid er elektronene i bevegelse i elektronskyen rundt atomene, og når to slike atomer kommer nær hverandre vil deres elektronskyer kunne påvirke hverandre slik atomene momentant polariseres og tiltrekker hverandre. Denne tiltrekningen er et resultat av fluktuasjoner, og kalles londonkrefter eller dispersjonskrefter.
Siden slike londonkrefter utveksles ved hjelp av fotoner som beveger seg med lysets hastighet, tar det en endelig tid for at de skal virke. Dersom de to atomene er for langt unna, vil det ene atomets elektronsky kunne forandre seg ganske mye før fotonene klarer å forplante seg dit fra det andre atomet. Dermed blir polarisasjonen av det første atomet liten, slik at londonkreftene blir forsvinnende små. Dette betyr at londonkrefter bare virker når atomene er svært nær hverandre og fotonene får tid til å forplante seg fra et atom til et annet.
Edelgassene er eksempel på dette. Dersom man kjøler ned edelgassene tilstrekkelig, kan atomene komme nær nok hverandre slik at londonkreftene blir sterke nok til at de danner væsker. Dette skjer for eksempel for helium ved 4,2 kelvin. Dersom molekyler eller atomer inneholder flere elektroner, blir londonkreftene sterkere, og da øker for eksempel smeltepunktet. Det betyr at tyngre edelgasser som xenon kan danne faststoff ved temperaturer under 161,3 kelvin.




Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.