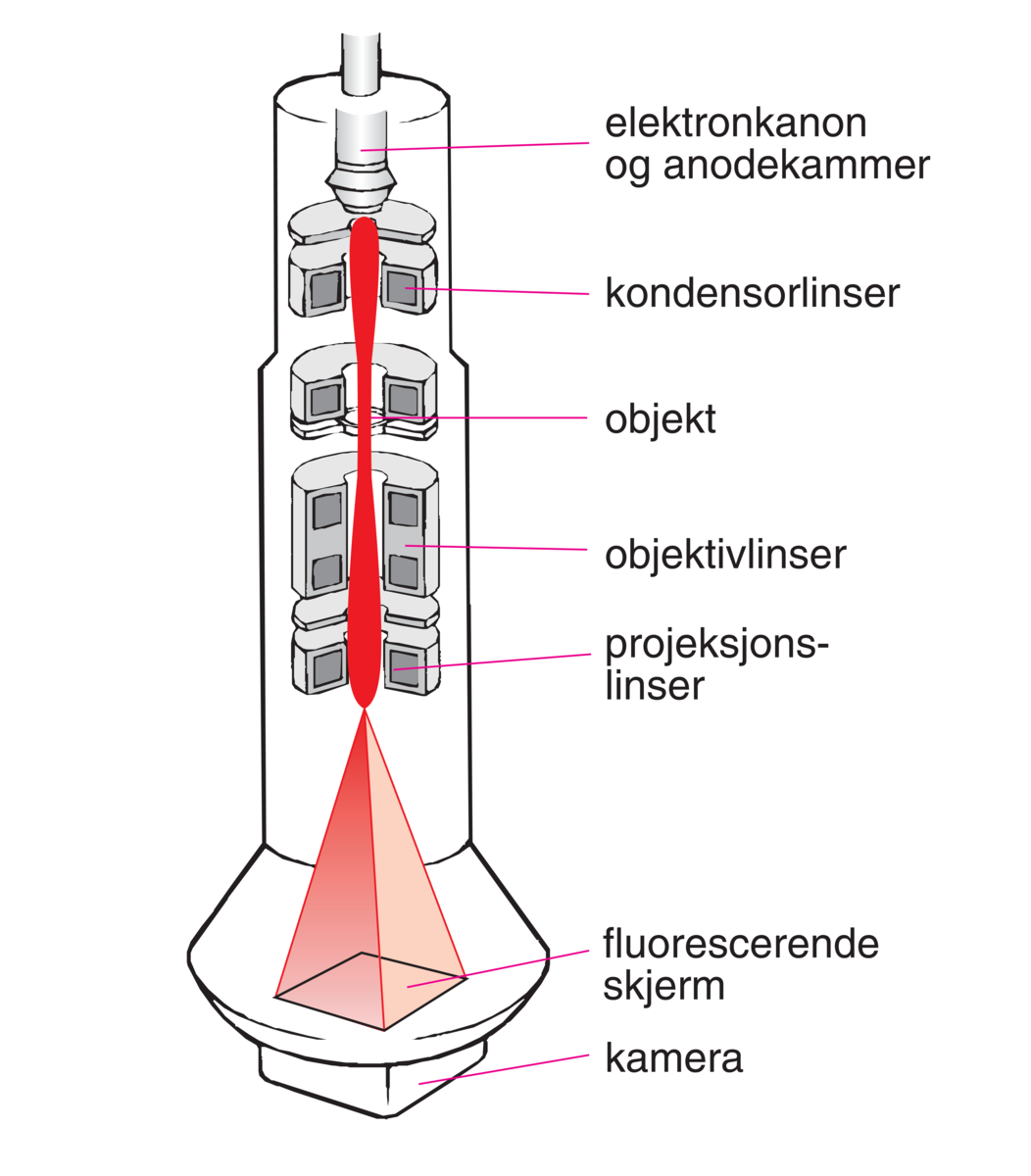
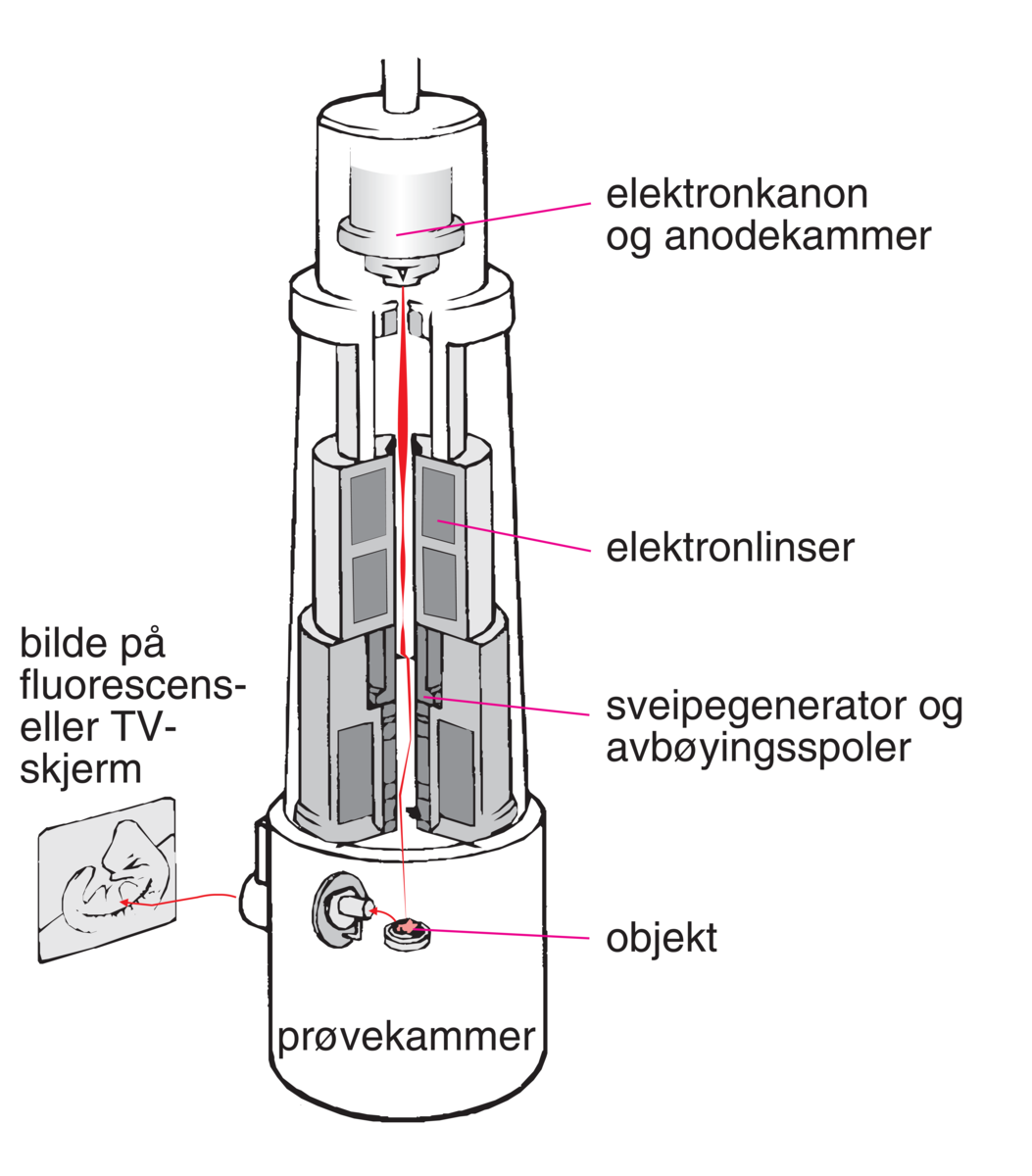
Transmisjonselektronmikroskopet (TEM, eng. Transmission Electron Microscope) er bygd opp analogt med et lysmikroskop for studier av tynne preparater ved gjennomlysning. Det består av strålingskilde, kondensorlinse, objektivlinse og en projeksjonslinse som tilsvarer et okular. En billedskjerm utgjør øyet som ser i et lysmikroskop. Strålingskilden er en elektronkanon, til erstatning for en glødelampe i lysmikroskopet.
Elektronene sendes ut (emitteres) fra en nålformet motstandsoppvarmet, glødende tråd av wolfram (eller lantanheksaborid, LaB6) som er gitt et høyt negativt elektrisk potensial (100–1000 kV) i forhold til jordede anodeplater plassert like under. De negativt ladede elektronene trekkes mot anoden. Geometrien til det elektriske feltet er slik at elektronene styres gjennom hull i anodeplatene og videre mot linsene og objektet i mikroskopet. Den konvergente strålebunten parallelliseres i kondensorlinsen og treffer objektet som ligger i objektivlinsens brennplan.
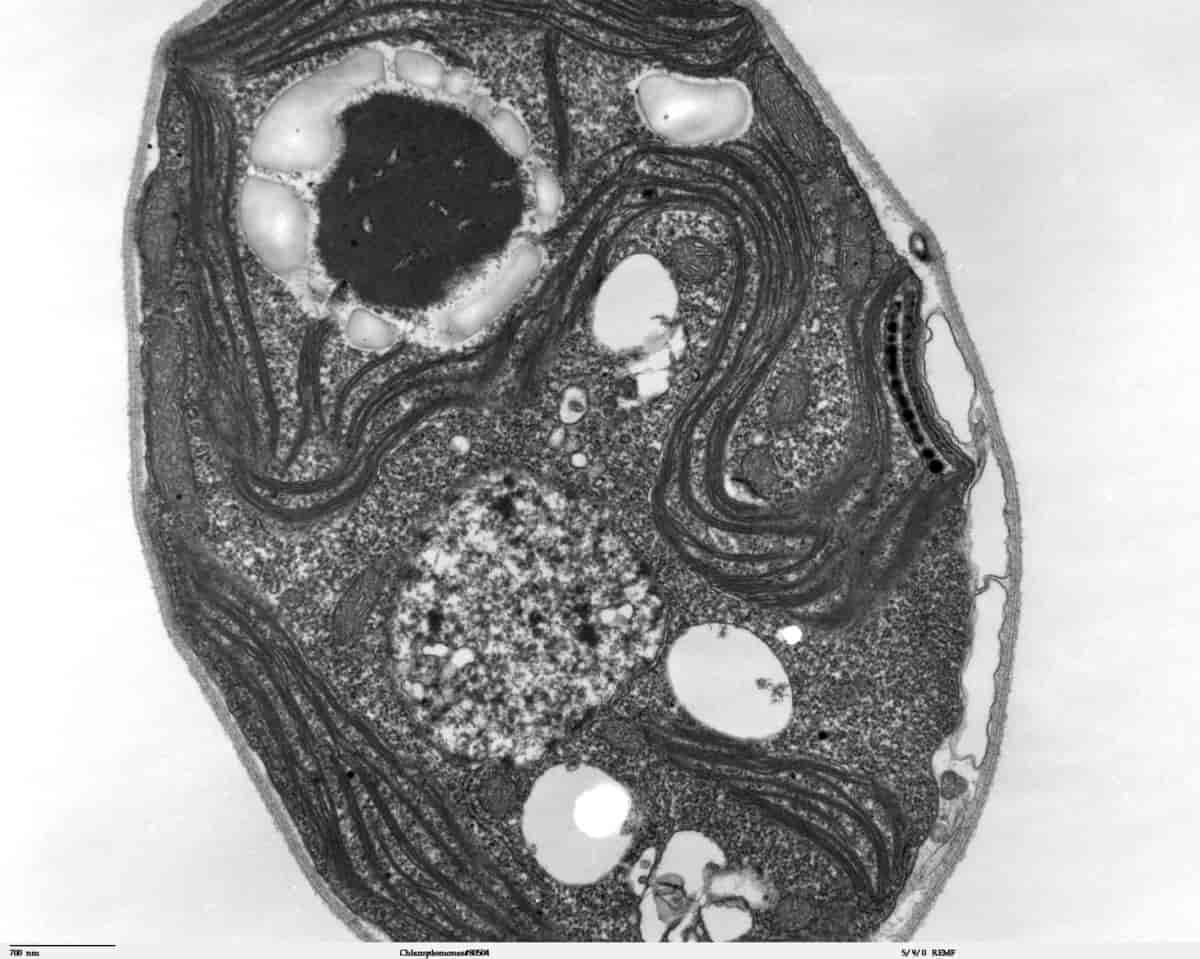
Det bilde som dannes blir forstørret i objektiv- og projeksjonslinsen, og selve bildet dannes på en fluorescerende skjerm som blir lysere der den treffes av mange elektroner. Alternativt treffer elektronene direkte en fotografisk film som dermed eksponeres, og et bilde fås ved fremkalling av filmen. Man får på denne måten et forstørret bilde av objektets indre struktur.
På grunn av elektronenes kraftige vekselvirkning med atomer/materie generelt, må hele strålegangen og preparatet befinne seg i høyvakuum. Dette betinger at prøvene man studerer er tørre og ikke dekomponerer under vakuumbetingelser. Av samme grunn må preparatene være særdeles tynne. For biologiske prøver, som vesentlig inneholder lette grunnstoffer, er ½0 000 mm (50 nm) en typisk tykkelse. For metaller, som består av tyngre atomer, bør preparatene være tynnere, for eksempel. 10 nm. Dette krever spesielle prepareringsmetoder, enten ved knusing eller ved etsing med elektrokjemiske eller fysikalske metoder. Alternativt kan ca. 50 nm tynne skiver lages ved snitting med en mikrotom ved hjelp av diamantkniv.
For at man skal få dannet et godt bilde, må det skapes kontrast når elektronstrålen passerer gjennom preparatet. Dette oppnås normalt direkte ved at elektronene spres i forskjellig grad, avhengig av tykkelse og hvilke typer av atomer som er til stede. Billedkontrast oppnås ved at bildet kun dannes av de elektroner som ikke blir spredt ut i ulike retninger.
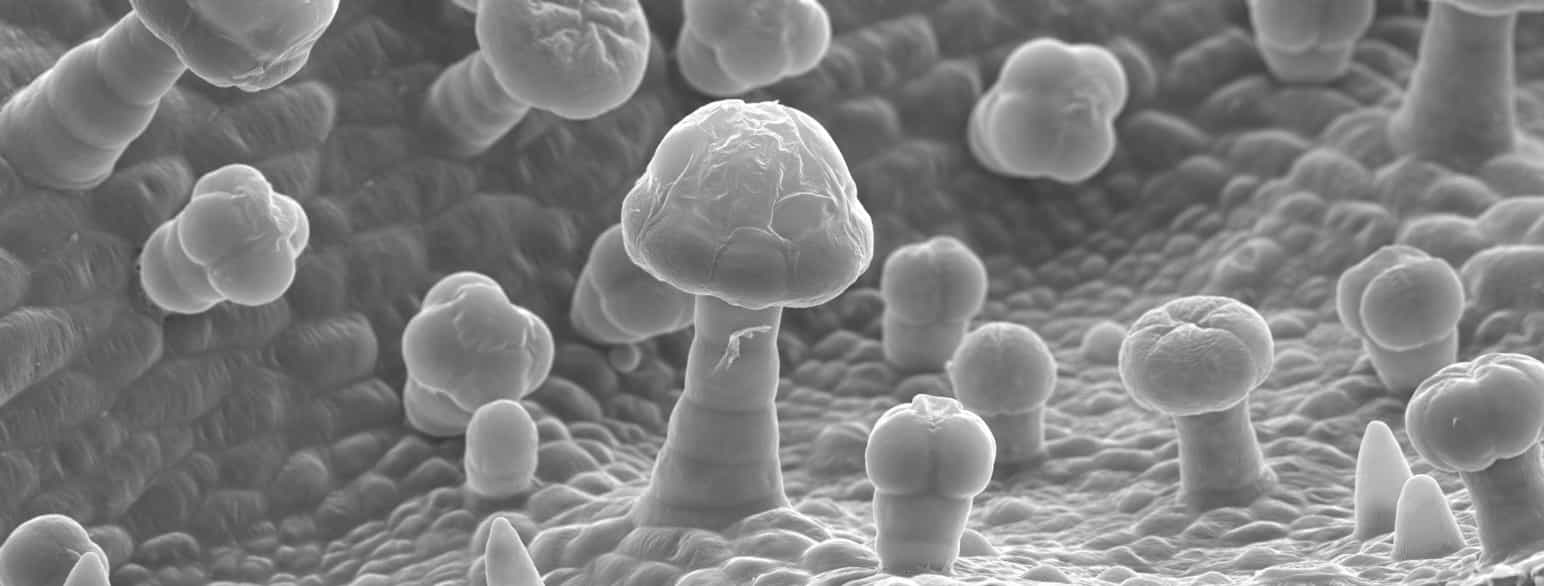
Preparater av meget små partikler som bakterier, røykstøv og liknende plasseres typisk på en tynn bærehinne av for eksempel plast, metall eller karbon. For tykke preparater kan man gjøre bruk av en avtrykksteknikk. Avtrykket vil da gjengi topografiske forhold i overflaten helt nøyaktig.
Avtrykksmaterialene er av samme type som bærehinnene. Slike avtrykkshinner vil være om lag like tykke og inneholde jevn fordeling av atomtyper. I utgangspunktet vil de gi liten kontrast, og spesielle skyggeleggingsteknikker benyttes derfor. Det samme gjelder for biologiske prøver. Slike prøver gis kontrast ved å behandle dem med osmiumtetraoksid, OsO4, eller med bly- og uranholdige salter.






Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.