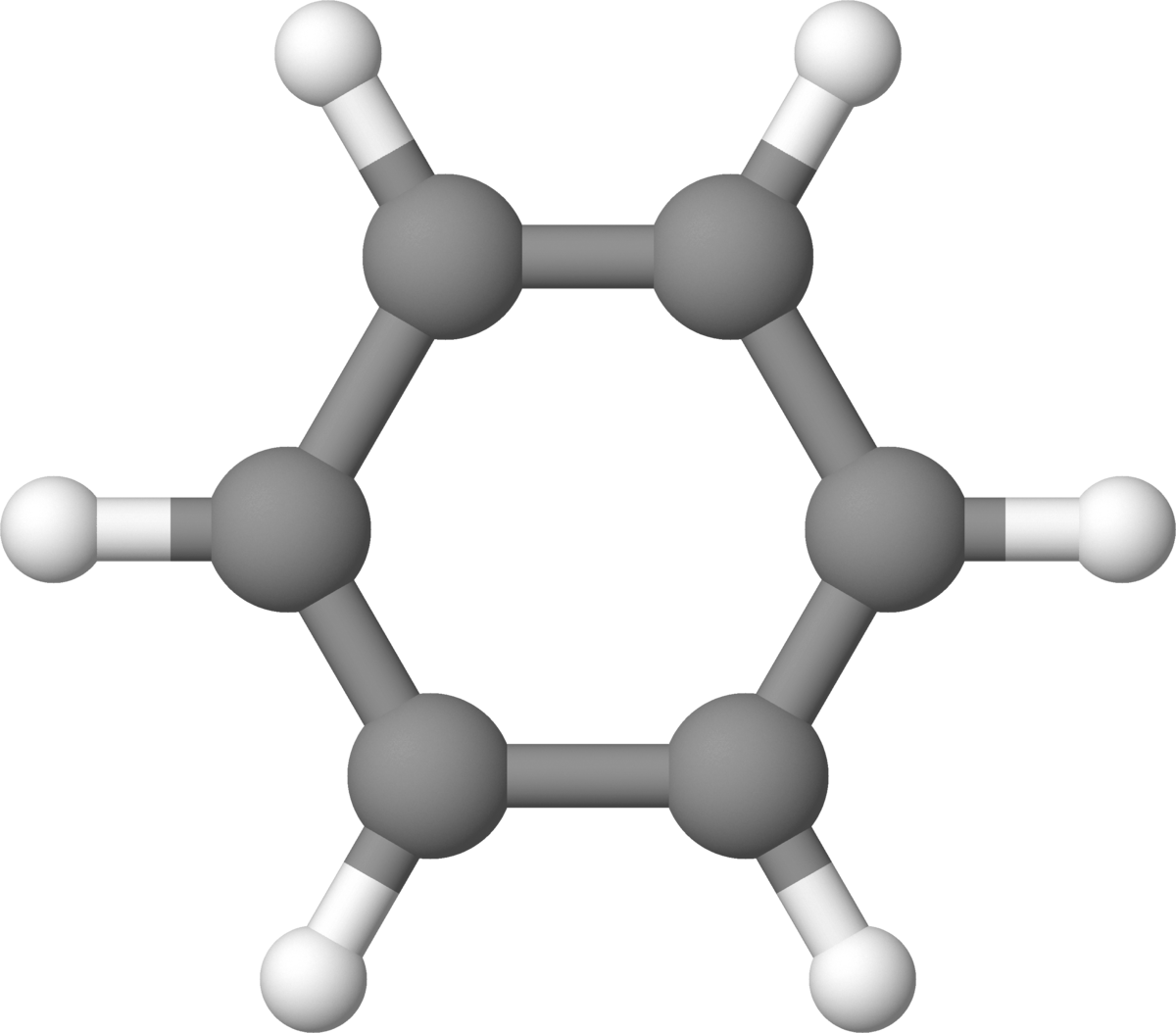
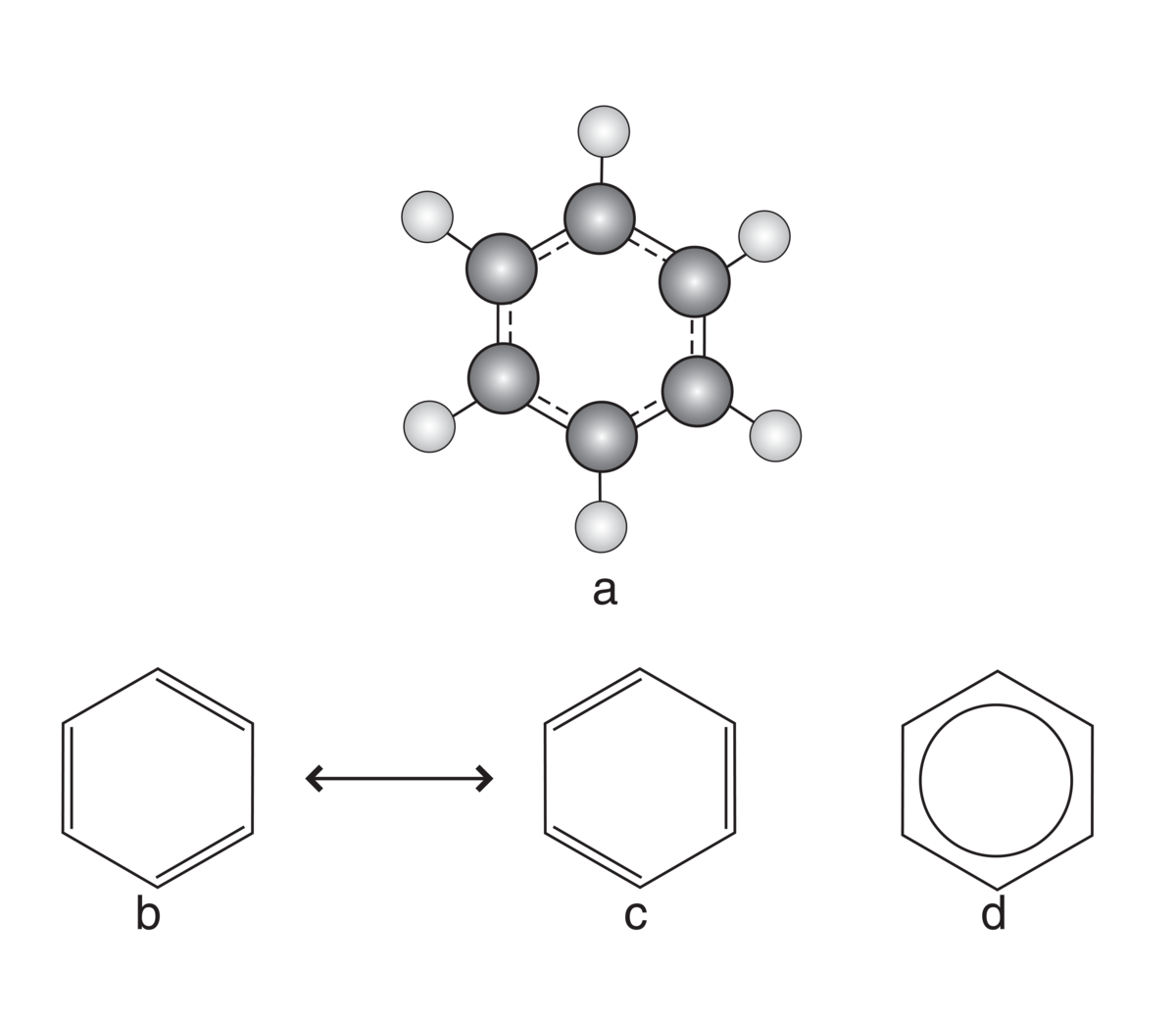
Benzen er en kjemisk forbindelse som er en fargeløs, sterkt lysbrytende væske med karakteristisk lukt. Den er giftig.
Faktaboks
- Norsk navn
- benzen
- Engelsk navn
- benzene
- Også kjent som
- forelda navn: benzol, bensol
- Uttale
- bensˈen
- Kjemisk formel
-
C6H6
- Stoffklasse
- aromatiske forbindelser
- Smeltepunkt
- 5,5 °C
- Kokepunkt
- 80,1 °C
- Tilstand
- væske




Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.