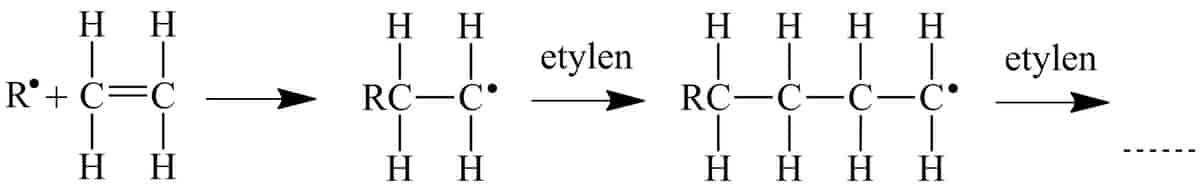
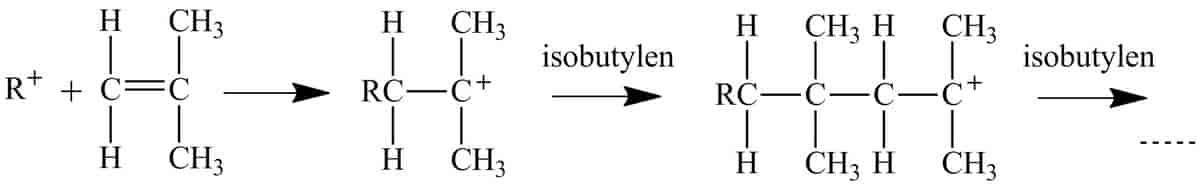
Polymerisasjon er kjemiske reaksjoner og prosesser der relativt små molekyler (monomerer) reagerer ved å binde seg sammen til mye større molekyler. De høymolekylære stoffene som dannes, kalles polymerer.
Faktaboks
- Uttale
- polymerisasjˈon
- Også kjent som
-
polymerisering
Polymerisasjon er den sentrale prosessen i kjemisk industri som produserer råstoffer til plast og syntetiske gummi-, lim-, lakk- og malingsprodukter fra petrokjemiske primærprodukter.





Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.