Fosforescens er en prosess hvor et stoff som absorberer energi, i en annen form enn varme, frigjør denne energien over tid i form av lys.
Faktaboks
- Uttale
- -sˈens
Dette skjer selv etter at tilførselen av den energien som omsettes til lys, er stanset.
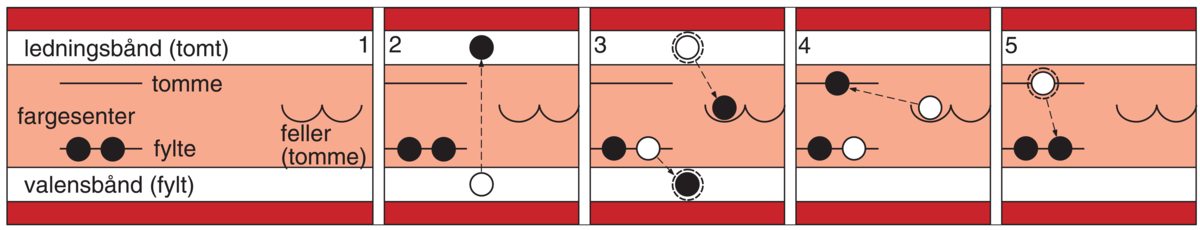
Fosforescens. Skjematisk fremstilling av fosforescens ved elektronbevegelsen i faste stoffer. Først vises energitilstandene omkring et fargesenter og hvordan disse er besatt før fosforet blir aktivisert (1). Ved tilførsel av energi kan et elektron løftes fra valensbåndet opp i ledningsbåndet (2) og faller derfra ned i en felle, samtidig som hullet i valensbåndet fylles med et elektron som før var bundet ved fargesenteret (3). I denne prosess frigjøres det mindre energimengder som går over til varme. Fra fellen føres elektronet ved varmebevegelse over til en tilstand der det kan slippe over i det ledige hull ved fargesenteret (4) og foretar denne siste overgang idet det sendes ut karakteristisk lysstråling (5).
Fosforescens er en prosess hvor et stoff som absorberer energi, i en annen form enn varme, frigjør denne energien over tid i form av lys.
Dette skjer selv etter at tilførselen av den energien som omsettes til lys, er stanset.
For å forstå årsaken til fosforescens, er det nyttig å kort beskrive den mer generelle klassen av fenomener som fosforescens tilhører. Denne klassen av fenomener kalles luminescens.
Ved luminescens blir elektroner i et stoff løftet fra en lavere til en høyere energitilstand på grunn av en annen ytre påvirkning enn varme. Eksempler på slik påvirkning er elektrisk energi, eksponering for lys eller en kjemisk eller biokjemisk reaksjon.
Fosforescens er et spesialtilfelle av luminescens hvor den ytre påvirkningen er lys: elektronene blir løftet til en høyere energitilstand på grunn av at de absorberer fotoner. Deretter faller elektronene over tid tilbake til et lavere energinivå samtidig som de sender ut lys.
Den tiden som elektronene bruker på å falle tilbake til det lavere energinivået, benyttes til å skille fosforescens fra andre former for luminescens, for eksempel det relaterte fenomenet fluorescens. Faller elektronene for eksempel tilbake igjen i løpet av den typiske levetid for eksiterte atomer, 10−8–10−7 sekunder, oppstår fluorescens.
Men i enkelte tilfeller fanges elektronene i såkalte feller. Dette er tilstander hvorfra de etter atomfysikkens lover har en veldig liten sannsynlighet for å kunne falle tilbake til den laveste energitilstanden. Ved termiske bevegelser kan imidlertid disse elektronene løftes opp av fellene og føres over i nærliggende energitilstander og derfra tilbake til utgangsstillingen under utsendelse av lys. Denne prosessen kalles fosforescens.
Det er karakteristisk for fosforescensen at den tiden lysutsendelsen varer, svekningstiden, er mye lengre enn den typiske levetid for eksiterte atomer. Mens man tidligere brukte betegnelsen fosforescens for alle luminiscerende prosesser med lang svekningstid, kalles det nå vanligvis langsom fluorescens når svekningstiden ikke viser temperaturavhengighet.
Opphører lysutsendelsen straks (i løpet av omtrent et mikrosekund), kalles altså prosessen i stedet fluorescens.
Fosforescens forekommer både i gasser, væsker og faste stoffer. Prosessen skjer ofte i flere trinn, idet et elektron løftes fra sin plass i gitterstrukturen eller molekylet og etterlater seg et hull der. Derpå kan enten hullet eller elektronet eller begge deler vandre inn mot et fargesentrum, oftest et fremmedatom, det vil si en tilsetning av et annet stoff. Både svekningstiden for lyset og fargen er sterkt avhengig av stoffet og av hvilke fremmedatomer som er til stede.
Stoffer som viser fosforescens, kalles fosforer.
Navnet fosforescens stammer fra grunnstoffet fosfor, som er selvlysende. Lyset fra fosfor skyldes paradoksalt nok ikke fosforescens, men en langsom oksidasjon som foregår under utsendelse av lys. Dette kalles for kjemiluminescens (se fosforoksider)

Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.