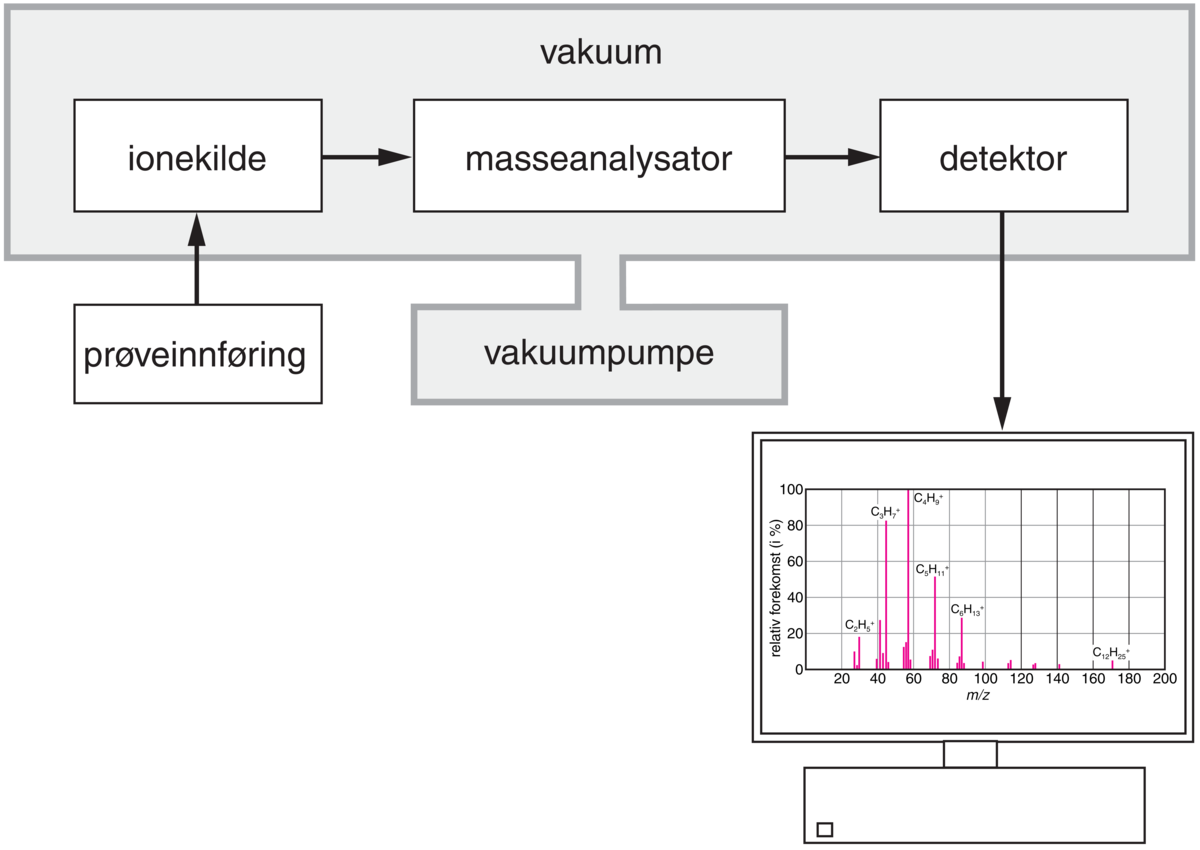
Massespektrometre finnes i mange ulike utførelser. Et moderne massespektrometer er alltid bygd opp av følgende hovedkomponenter:
- prøveinnføringssystem
- ionekilde
- masseanalysator
- detektor
- datasystem
Prøven som skal analyseres, kan være gass, væske eller fast stoff. For tradisjonelle ioniseringsteknikker må prøven omdannes til gass før den overføres til ionekilden hvor ioniseringen finner sted, for eksempel ved at prøvemolekylene bombarderes med en stråle av elektroner. Deretter ledes ionene inn i en masseanalysator som vanligvis består av et arrangement av elektriske og/eller magnetiske felter. Det er her ionene separeres ut fra forskjeller i m/z-verdi.
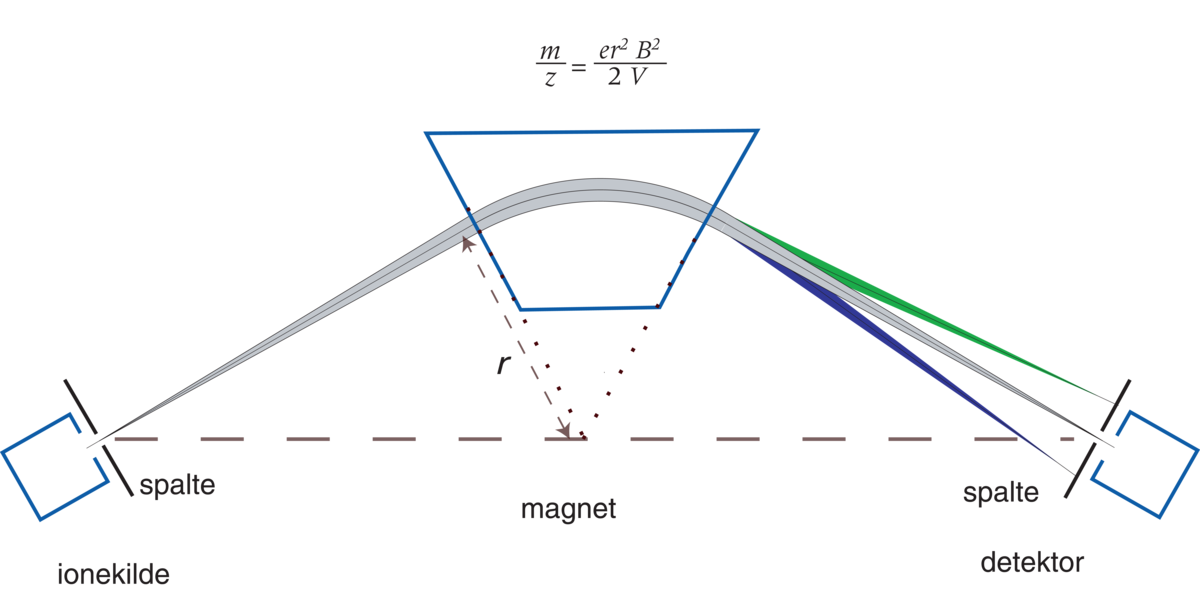
Det finnes forskjellige typer masseanalysatorer. De vanligste er magnetsektor-, kvadrupol-, flygetid- og ionefelleanlysator. Før ionene blir ført inn i en magnetsektoranalysator, ledes de først gjennom et elektrostatisk felt (akselerasjonsfelt) hvor de tilføres energi og deretter, ved påvirkning av elektriske felter, blir samlet til en skarp stråle som så ledes inn i et sirkelsektorformet homogent magnetfelt. I magnetfeltet avbøyes ionene, og de følger en sirkelbane hvor radiusen er avhengig av ionets m/z-verdi. Bare ioner med en bestemt baneradius vil passere rett gjennom masseanalysatorens utgangsspalte og treffe detektoren som sitter rett bak spalten.
Ved å variere magnetfeltstyrken kan man styre hvilke ioner (det vil si hvilke m/z-verdier) som vil passere spalten og deretter detekteres. Instrumentet kan dermed programmeres til å sveipe over et ønsket m/z-område. Et fullstendig sveip over alle m/z-verdiene tar vanligvis under et sekund.
Detektoren gir en elektrisk respons for hver m/z-verdi. Det finnes flere typer detektorer, inkludert mangekanalsdetektorer, som muliggjør simultan deteksjon av ionene.
For å oppnå god masseoppløsning, det vil si å kunne skille ioner med liten forskjell i m/z-verdi, benytter man en elektrostatisk analysator i tillegg til magnetsektor-masseanalysator. Slike instrumenter kalles dobbelfokuserende eller høytoppløsende instrumenter.
De forskjellige typene magnetsektor- og dobbeltfokuserende instrumenter varierer med hensyn til utformingen av avbøyningsfeltene og plasseringen av de elektriske og magnetiske feltene i forhold til hverandre. De bygges dels for å dekke et stort m/z-område og dels for å oppnå god oppløsning. Mattauchs massespektrograf og Niers massespektrometer er kjente dobbeltfokuserende instrumenter med meget høy oppløsning. Fourieromvandlingsmassespektrometer er et annet eksempel.
Foruten høy masseoppløsning er det viktig at et massespektrometer er stabilt, slik at magnetiske og elektriske felter ikke varierer med tiden eller at metalldelene i instrumentet får anledning til å krympe/vokse med varierende temperatur i lokalet. Dermed er det mulig å bestemme m/z-verdier, og dermed molekylvekter, med meget stor nøyaktighet.
Man har utviklet mange typer av ionekilder som dekker ulike analysebehov. For bestemmelse av molekylmasser er det for eksempel gunstig å velge en ionekilde som gir liten eller ingen grad av fragmentering (kun ionisering); for bestemmelse av grunnstoffer velger man ionekilder som ideelt gir en total dekomponering av prøven i frie enverdige ioner (se ICP); ved identifisering av en ukjent forbindelse velger man en ionekilde som gir relativt høy grad av fragmentering. Ved mye fragmentering fås en sikrere identifikasjon, fordi det da er mindre sannsynlig at flere molekyler har samme fragmenteringsmønster. Det finnes også dataprogrammer som kan hjelpe med strukturoppklaringen.
Signalet fra detektoren gis vanligvis i form av et massespektrum (m/z-verdi som funksjon av ionestrøm) som registreres på en skjerm. Massespekteret gir blant annet grunnlag for strukturbestemmelse av molekyler og identifisering av ukjente forbindelser. Ved kvantitative bestemmelser måler man ionestrømmen ved en gitt m/z-verdi for den aktuelle forbindelsen eller grunnstoffet.




Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.