Kritisk tilstand for et stoff ved overgang mellom gass- og væskeform er gitt ved tilstandens kritiske temperatur og trykk.
Faktaboks
- Uttale
- krˈitisk tilstand
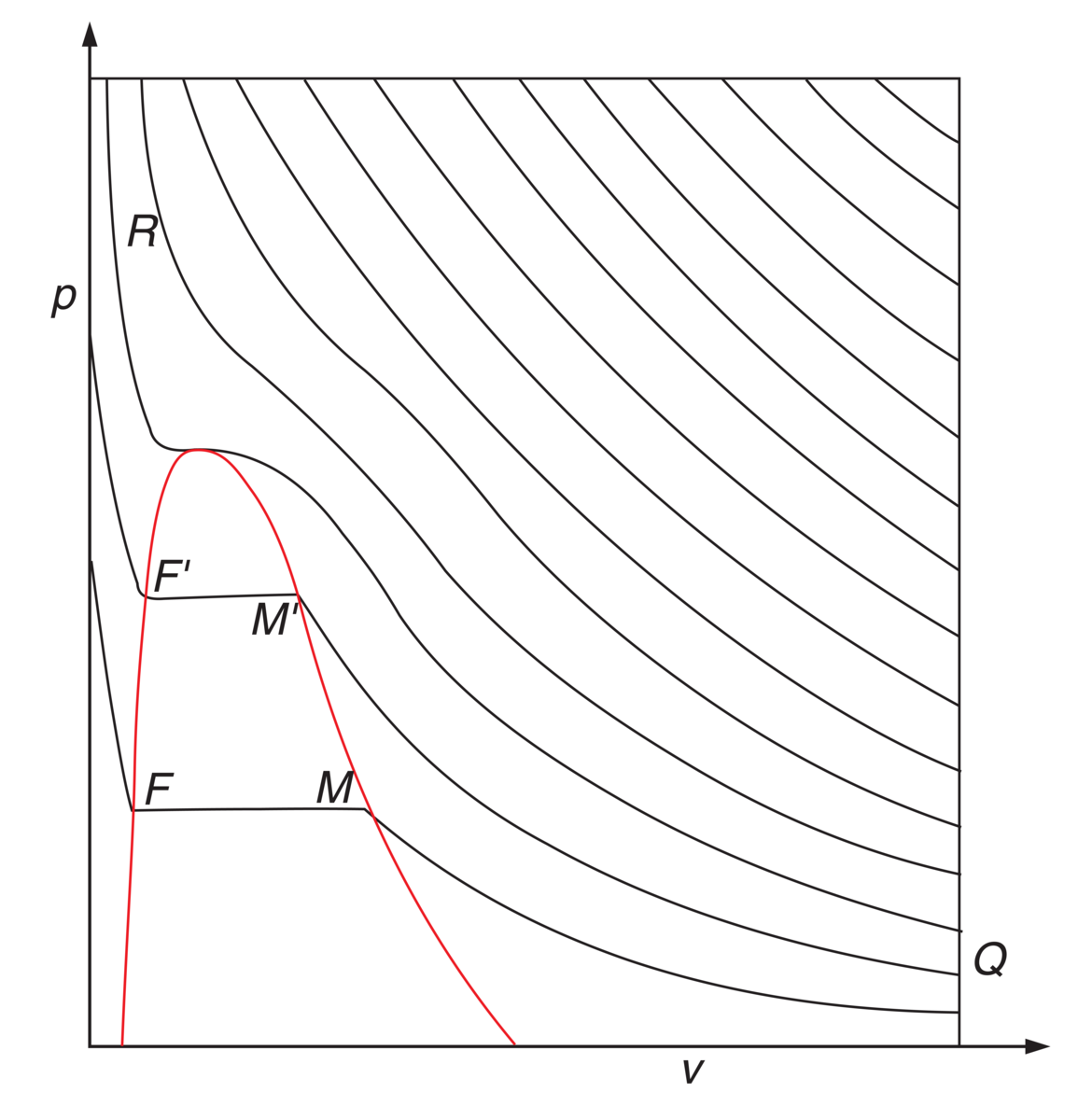
De fleste stoffer kan ved passende valg av trykk og temperatur bringes over i alle tre aggregattilstander: fast, flytende og gassformig. Ved trippelpunktet kan disse fasene eksistere sammen, og dette skjer for eksempel ved 0,01 °C for vann. Øker man trykket og temperaturen videre, vil man til slutt komme til et endepunkt i fasediagrammet som kalles det kritiske punktet, der stoffet er i en kritisk tilstand der man ikke kan skille væske- og gassformen.
Over en viss temperatur er det ikke mulig å bringe en gass over i væskeform, selv om trykket blir aldri så høyt. Denne maksimale temperaturen for væsken kalles stoffets kritiske temperatur, og det trykk som må til for å bringe gassen over i væskeform ved denne temperaturen, kalles stoffets kritiske trykk. Når stoffet har denne temperaturen og utsettes for dette trykket, sies stoffet å være i sin kritiske tilstand.
Dersom trykket og temperaturen er er større enn de kritiske verdiene, får man et superkritisk fluid. I et slikt fluid kan man ikke skille mellom væske og gassform, og overflatespenningen blir svært liten. Slike superkritiske fluider kan brukes til å trekke stoffer ut av et materiale, til fremstilling av kjemikalier og til impregnering av materialer.
Kritisk temperatur og trykk for en del stoffer er gitt i tabellen nedenfor. Fenomenet ble klarlagt av den irske fysiker Thomas Andrews i hans studier av karbondioksid 1869-76.




Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.