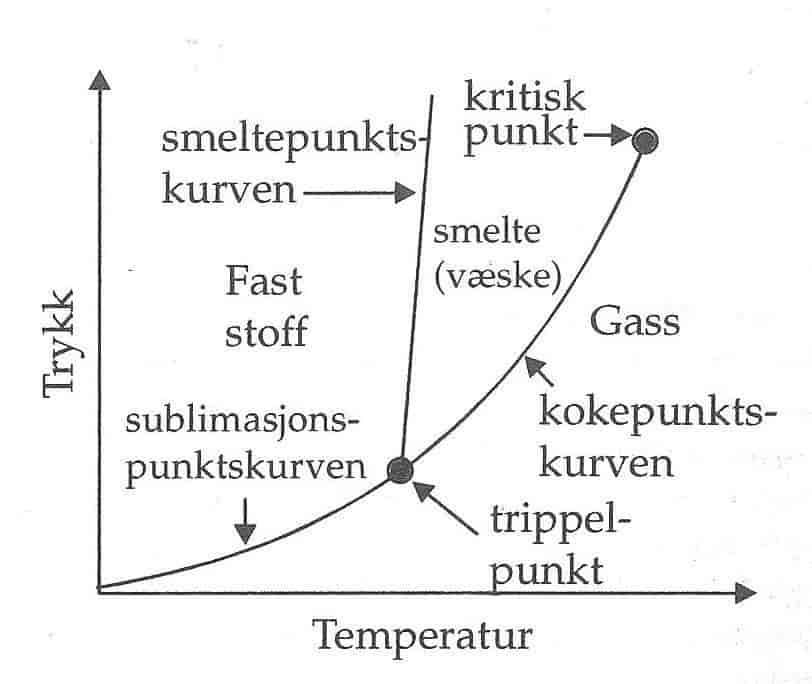
Figur 1 viser et eksempel på et enkelt fasediagram for en kjemisk forbindelse A. A kan eksistere i tre faser: fast stoff, smelte og gass. På førsteaksen (x-aksen) er temperaturen angitt, og på andreaksen (y-aksen) trykket.
I fasediagrammet er det tegnet tre kurver:
-
Sublimasjonskurven viser hvordan damptrykket av det faste stoffet i likevekt med sin damp (en gass) endrer seg med temperaturen.
-
Smeltepunktskurven viser hvordan damptrykket av det faste stoffet i likevekt med sin smelte (en væske) endrer seg med temperaturen.
-
Kokepunktskurven viser hvordan kokepunktet for smelten i likevekt med sin damp endrer seg med temperaturen.
Trippelpunktet er den temperaturen og det trykket hvor de tre fasene av A: fast stoff, smelte og damp, er til stede samtidig og i likevekt.
Det kritiske punktet er den temperaturen og det trykket hvor det er slutt på smelten, og vi ikke lenger kan skille mellom smelte og damp.
Fasediagrammet i figuren passer med fasediagrammet for karbondioksid. Trippelpunktet er ved et trykk på 5,2 atm og en temperatur på -56,6 °C. Det kritiske punktet er ved et trykk på 73 atm og en temperatur på 30 °C.
Fasediagrammet for H2O er noe forskjellig fra dette. Her skrår smeltepunktskurven den andre veien, det vil si at smeltepunktet for is avtar med økende trykk. Dessuten er det 9 faste modifikasjoner av is. Trippelpunktet er ved et trykk på 0,0060 atm (611,7 Pa) og en temperatur på 0,01 °C.




Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.