Ioneligning er en kjemisk reaksjonsligning som beskriver en reaksjon mellom ioner.
Faktaboks
- Uttale
- iˈoneligning
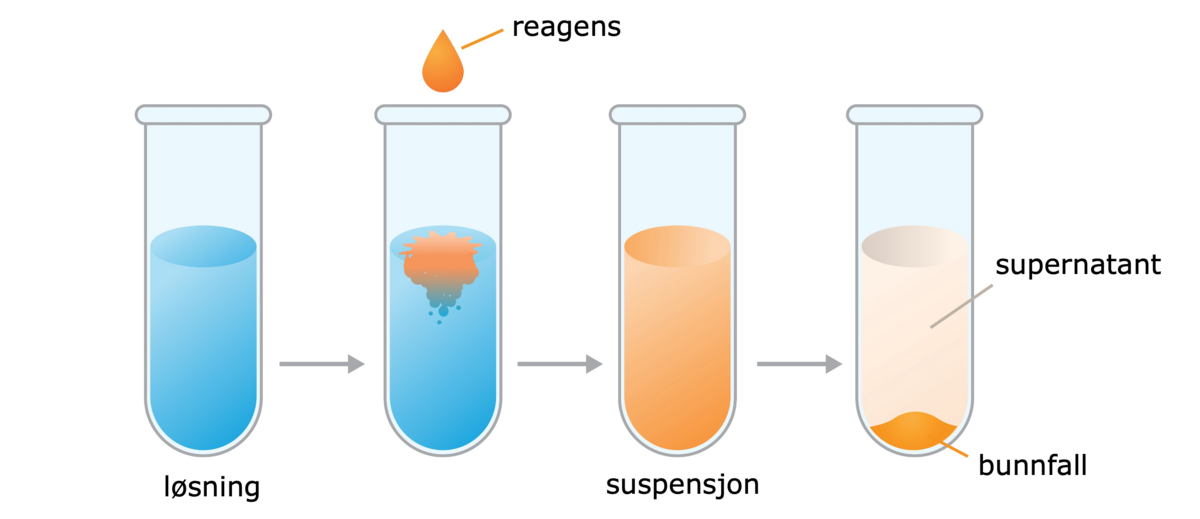
I røret til venstre er det en klar løsning. I neste rør til høyre tilsettes en reagens, det vil si en løsning med andre kjemiske stoffer. De to løsningene blander seg og danner en suspensjon i tredje rør. I røret helt til høyre har suspensjonen fått stå noe tid, slik at det har skjedde en fellingsreaksjon. I bunnen ligger bunnfallet, over dette er supernatanten.
Ioneligning er en kjemisk reaksjonsligning som beskriver en reaksjon mellom ioner.
Dersom man tilfører en løsning med sølvnitrat (AgNO3) til en løsning med natriumklorid (NaCl), dannes øyeblikkelig et hvitt bunnfall av fast sølvklorid, AgCl. Reaksjonen kan beskrives med følgende ligning:
\[\ce{NaCl + AgNO3 -> NaNO3 + AgCl}\]
Reaksjonen kan også skrives på en annen og mer korrekt måte. For både natriumklorid og sølvnitrat foreligger egentlig oppløst i form av ioner i vannet. En bedre ligning er derfor:
\[\ce{Na+(aq) + Cl^{-}(aq) + Ag+(aq) + NO3^{-}(aq) -> Na+(aq) + NO3^{-}(aq) + AgCl(s)}\]
Her viser (aq) at ionene er løst i vann, og (s) viser at sølvklorid er et fast stoff.
Dersom man sløyfer de ionene som opptrer på begge sider av reaksjonspilen, fås ioneligningen:
\[\ce{Cl^{-}(aq) + Ag+(aq) -> AgCl(s)}\]
Alle tre ligningene er balansert, da det er like mange atomer/ioner av hver sort på hver side av pilen. Ionene som ikke deltar i reaksjonen, og som er sløyfet i den balanserte ioneligningen, kalles tilskuerioner.
Kloridioner og sølvioner i en vannløsning vil reagere og danne sølvklorid uansett hvilke forbindelser ionene kommer fra. Kloridionene kan for eksempel stamme fra saltsyre (HCl(aq)), natriumklorid eller hvilket som helst annet løselig klorid.

Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.