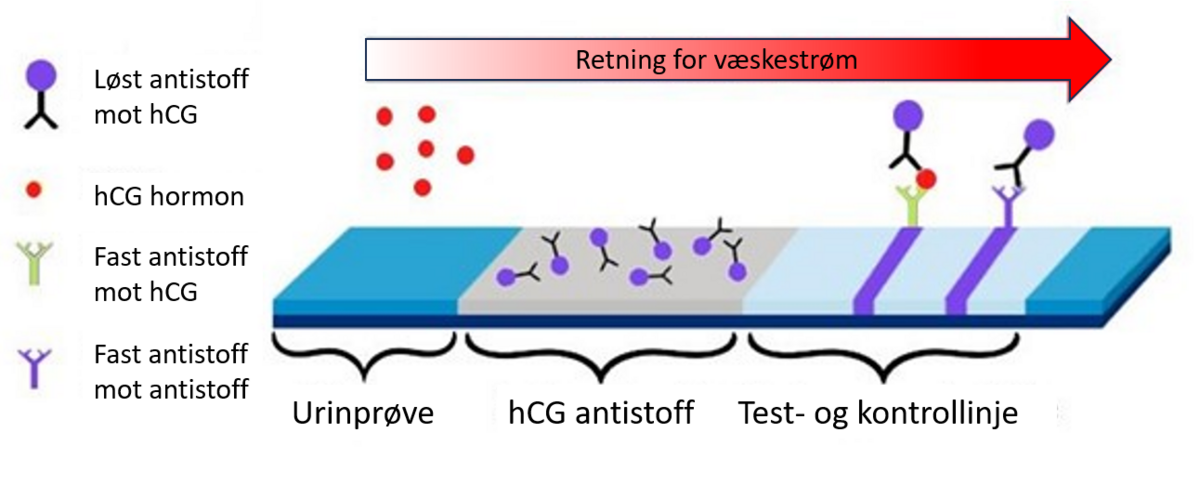
Lab-on-a-chip (LOC) er små brikker, typisk kun noen kvadratcentimeter i størrelse, som kan brukes til oppgaver som normalt må gjøres i et laboratorium. Teknologien brukes allerede i graviditetstester og blodsukkermålere, men har fremdeles mye rom for videre utvikling. Det langsiktige målet for LOC er å lage et analysesystem som kan gjøre tusenvis av tester, og som kun krever en dråpe væske. Dette har i faglitteraturen fått navnet Micro Total Analysis System, eller μTAS.
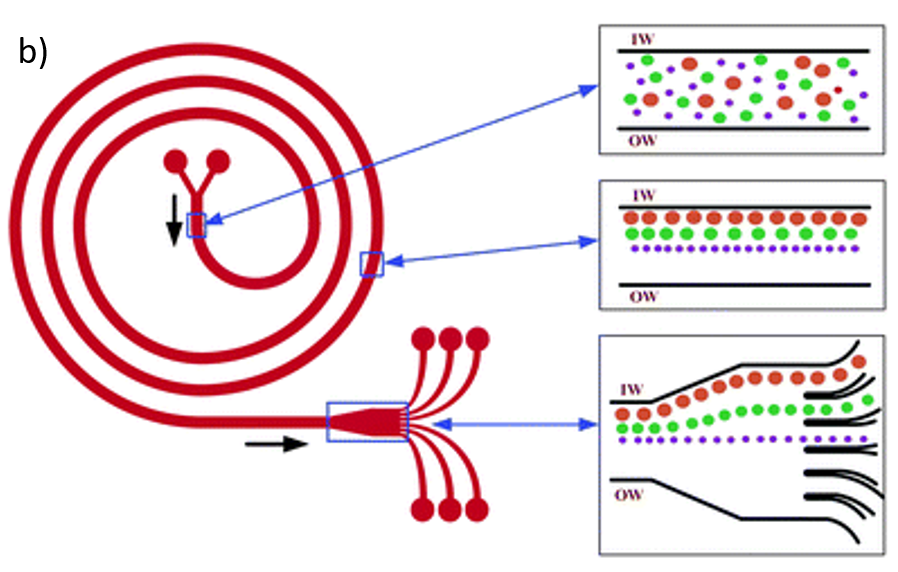
For å muliggjøre slike systemer kreves det at man jobber med veldig små væskevolum. Når reaksjonsvolumet er i mikro- til pikoliter-området, kan man nemlig regulere temperatur raskere, øke væsketransport og ha presis kontroll over væskestrøm. Dette betyr at flere laboratorietester blir enklere, raskere og mer presise. En annen fordel er at det kreves mindre reagens og kjemikalier sammenliknet med konvensjonelle tester, noe som kan gjøre LOC til et mer økonomisk alternativ. LOC anvendes mye i biologi og legevitenskap, men det finnes også andre bruksområder.





Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.