En indikator er en kjemisk forbindelse som brukes til å påvise om andre forbindelser er til stede. Vanligvis er det et stoff som skifter farge når det kommer i kontakt med en bestemt type stoff eller ett bestemt stoff.
Faktaboks
- Uttale
- indikˈator
- Etymologi
- til indikere
Et eksempel er at jod gir en kraftig blåfarge når det kommer i kontakt med stivelse. Stivelse kan derfor brukes som indikator for jod. Radioaktive indikatorer er isotoper som benyttes til studier av kjemiske reaksjoner.
Ved titrering benyttes fargeindikatorer til påvisning av endepunktet i titreringen.
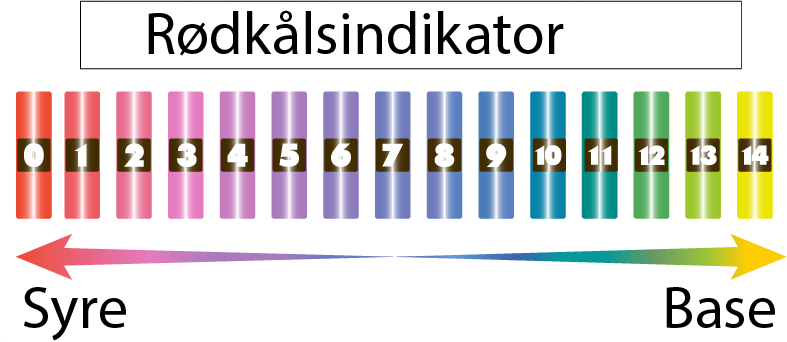
- I syre–base-titreringer benyttes pH-indikatorer som skifter farge innen et lite pH-intervall.
- I red–oks-titreringer benyttes indikatorer som skifter farge innen et lite potensialområde.
- I kompleksometrien brukes indikatorer som har forskjellig farge i kompleks og fri tilstand.




Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.