Glykol er en kjemisk forbindelse som er en fargeløs, litt viskøs væske med søt smak. Glykol brukes i frostvæske for å senke frysepunktet og som løsemiddel. Væsken er blandbar med vann i alle forhold og har kokepunkt 197 °C og smeltepunkt −17 °C.
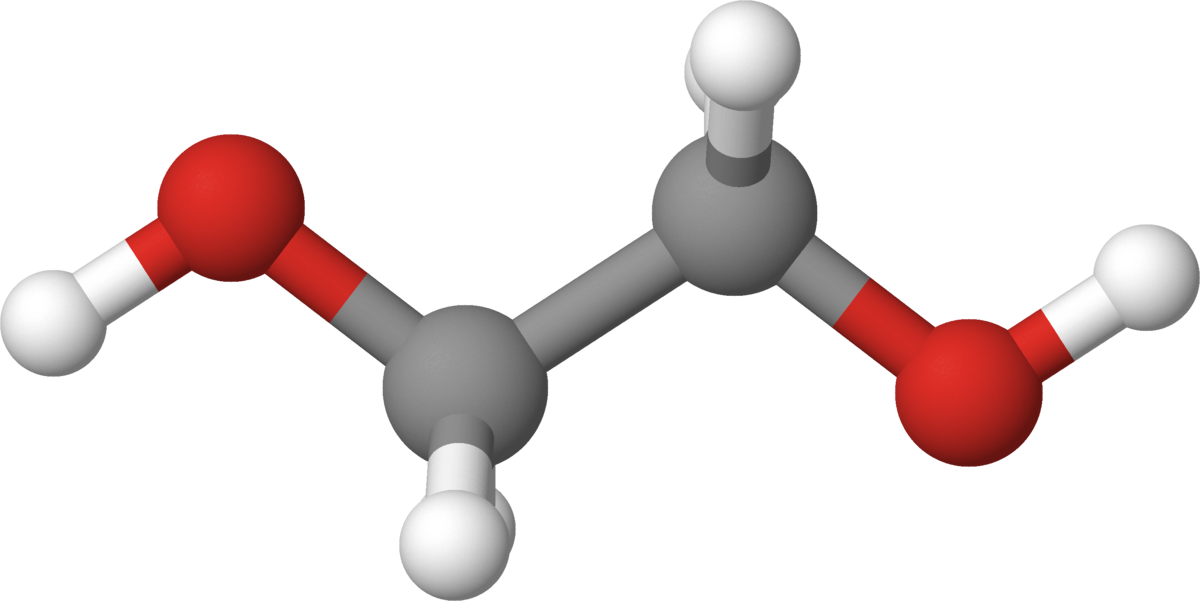
Glykol er den enklest bygde forbindelsen av stoffklassen glykoler. Glykol kalles også etylenglykol, den kjemiske betegnelsen er 1,2-etandiol, og kjemisk formel er HOCH2–CH2OH.





Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.