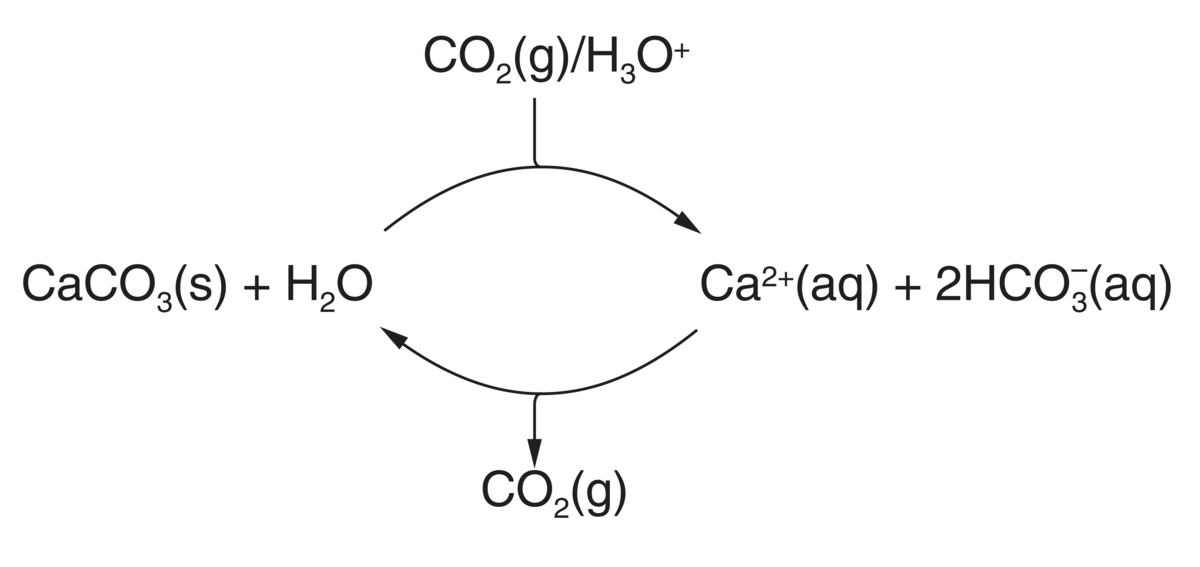
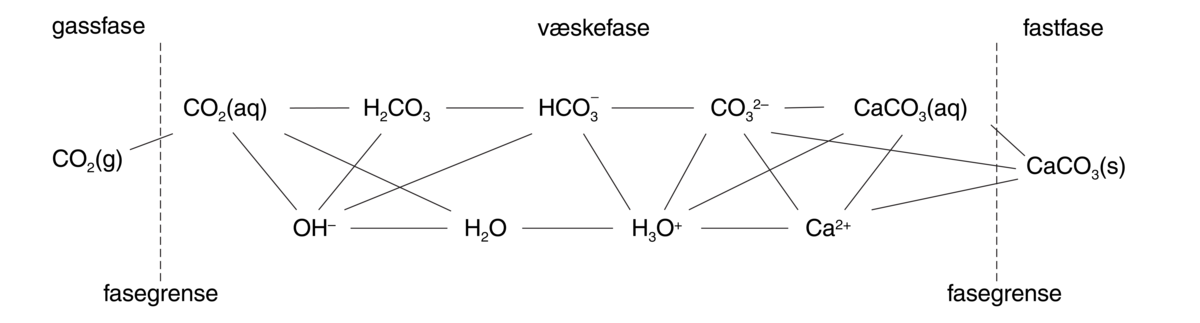
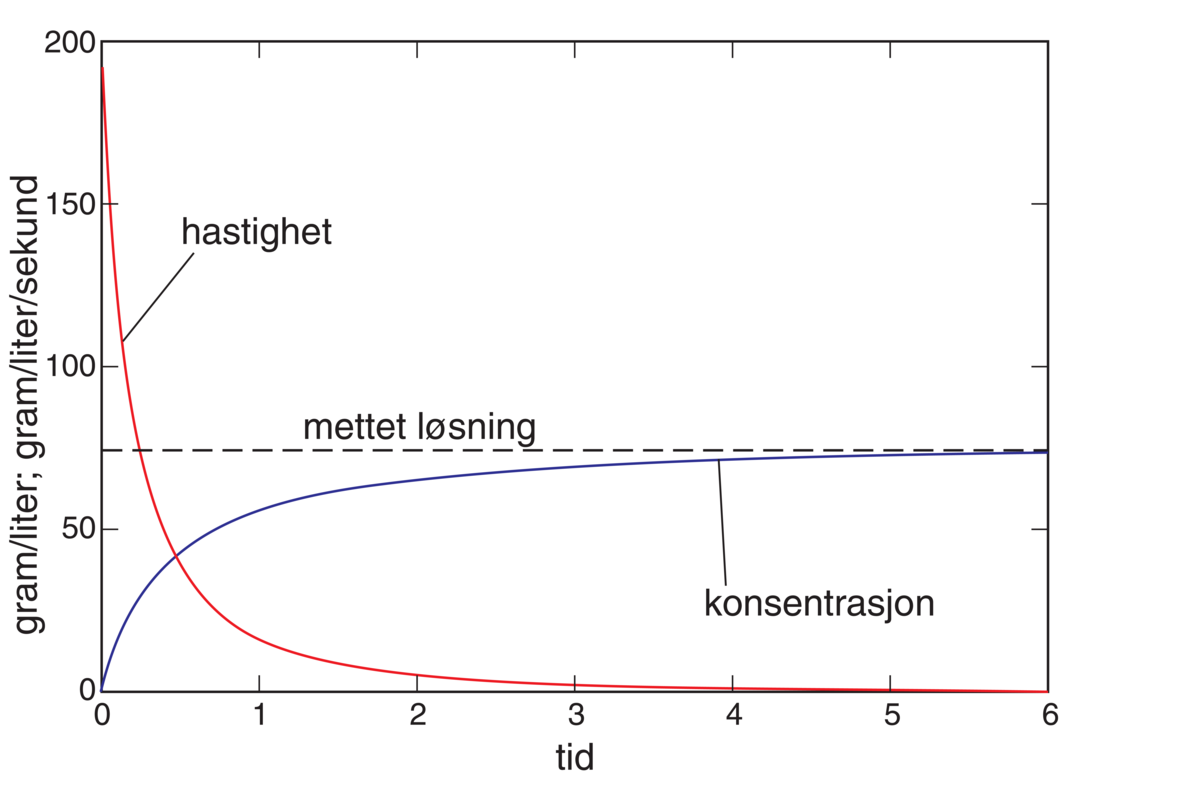
Karbonatkinetikk, vitenskapelig fagfelt knyttet til oppløsning og utfelling av kalsiumkarbonat i naturlig vann. Dette er viktige prosesser i mange geologiske og biologiske miljøer, blant annet fører oppløsningsprosessen til dannelse av karst, mens utfellingsprosessen fører til dannelse av kalktuff, speleothemer og til sementering (diagenese) av løsmasser.
Faktaboks
- Uttale
- karbonˈatkinetˈikk




Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.